In der am Universitätsklinikum Köln durchgeführten retrospektiven Studie wurden zwei Kriterien zur radiologischen Beurteilung des Therapieansprechens, iRECIST und RECIST 1.1., verglichen. Der Vergleich erfolgte in einer Gruppe von Patient:innen, die zur Behandlung des Melanoms oder nicht-kleinzelligen Lungenkarzinoms Immun-Checkpoint-Inhibitoren erhielten.
Ziel war es, herauszufinden, welche Methode besser geeignet ist, um atypisches Therapieansprechen auf diese Immuntherapien in der klinischen Praxis zu erfassen. Eingeschlossen wurden 252 Patient:innen (150 Männer, 102 Frauen) mit Melanom bzw. nicht-kleinzelligem Lungenkarzinom.
RECIST 1.1 ist der bewährte Standard zur Bewertung des Therapieansprechens solider Tumore in klinischen Studien, hat jedoch Schwächen bei der Beurteilung von Immuntherapien, da es atypisches Therapieansprechen wie die sogenannte Pseudoprogression nicht erfasst.
Pseudoprogression beschreibt das Phänomen, dass Tumoren zunächst wachsen, bevor sie auf die Behandlung ansprechen. iRECIST wurde speziell entwickelt, um diese Herausforderungen zu bewältigen und atypische Ansprechmuster wie die Pseudoprogression besser zu erfassen.
Die Studie brachte folgende Ergebnisse:
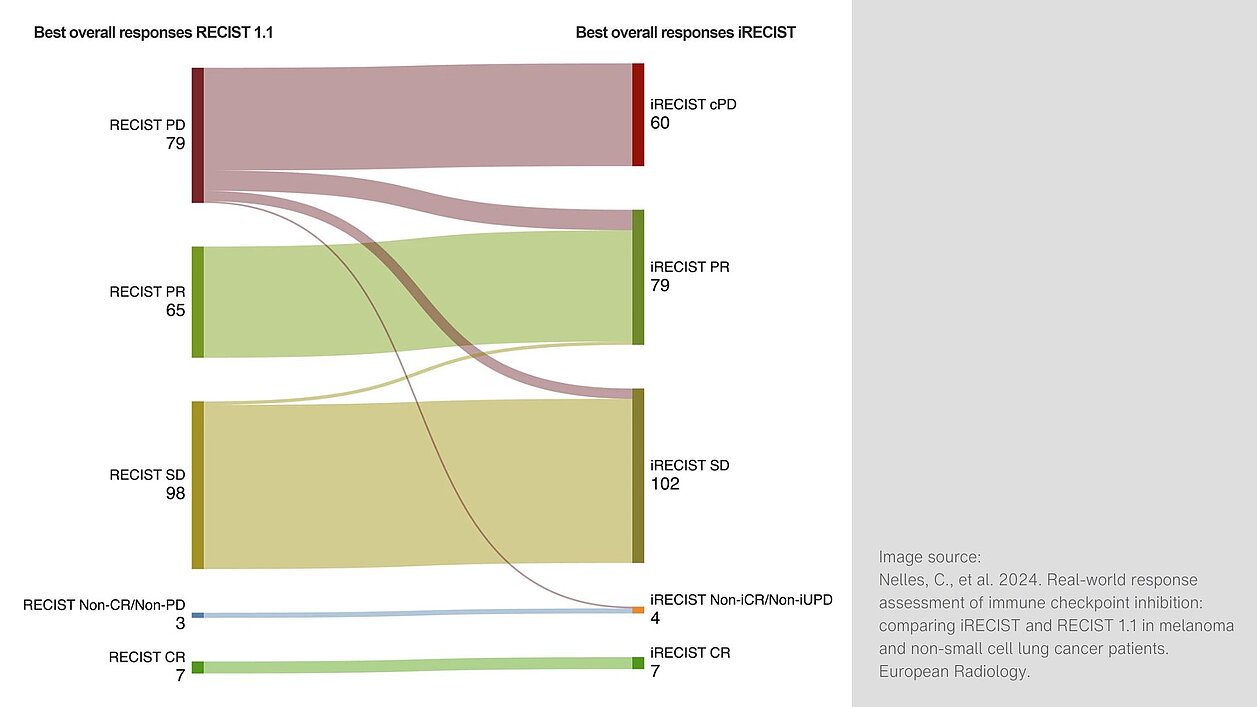
- Von den Patient:innen, die laut RECIST 1.1 ein Fortschreiten der Krankheit (PD) zeigten, bestätigte iRECIST bei 33,6% der Fälle die Progression nicht.
- iRECIST stellte eine höhere Gesamtansprechrate (ORR) von 34,1% im Vergleich zu 28,5% bei RECIST 1.1 fest. Die resultierende Krankheitskontrollrate (DCR) war ebenfalls höher: 74,6% bei iRECIST im Vergleich zu 67,4% bei RECIST 1.1.
- Die Zeit bis zum Fortschreiten der Krankheit (TTP) war in der Auswertung des Therapieansprechens mit iRECIST signifikant länger als bei RECIST 1.1 (durchschnittlich 618,3 Tage bei iRECIST gegenüber 538,1 Tagen bei RECIST 1.1).
Die Ergebnisse zeigen, dass iRECIST besser geeignet ist, um atypisches Therapieansprechen auf Immuntherapien zu erfassen, insbesondere bei Patient:innen mit Pseudoprogression. Dies kann verhindern, dass Patient:innen fälschlicherweise ein fehlendes Therapieansprechen attestiert und ihre Behandlung frühzeitig beendet wird. Zukünftige Studien sollten prospektiv untersuchen, ob das Erfassen solcher Ansprechmuster den potentiellen Nachteil einer verzögerten Diagnose eines Krankheitsfortschritts aufgrund der Notwendigkeit einer kurzfristigen Verlaufskontrolle zu dessen Bestätigung, aufwiegt.
Die Adaption von iRECIST in die klinische Praxis könnte dazu beitragen, die Ergebnisse von Immuntherapien zu verbessern, indem eine genauere radiologische Beurteilung des Therapieansprechens ermöglicht wird.
Lesen Sie die Originalpublikation hier.
Nelles, Christian, et al. 2024. „Real-world response assessment of immune checkpoint inhibition: comparing iRECIST and RECIST 1.1 in melanoma and non-small cell lung cancer patients.” European Radiology.