Die aktuelle Studie „Artificial intelligence for TNM staging in NSCLC – a critical appraisal of segmentation utility in [18F]FDG PET/CT“ untersucht kritisch, welchen klinischen Mehrwert künstliche Intelligenz (KI) für die Segmentierung des nicht-kleinzelligen Lungenkarzinoms (NSCLC) bietet.
Während die überwiegende Zahl wissenschaftlicher Arbeiten in diesem Themenbereich primär technische Outcomes analysiert, sollte in dieser translationalen Arbeit gezielt untersucht werden, inwieweit sich formal vielversprechende Segmentierungsergebnisse auf klinisch relevante Punkte wie die korrekte Erkennung von Läsionen, die Klassifikation (TNM/UICC) und letztlich Therapieentscheidungen auswirken.
Studiendesign und Methodik
Die retrospektive Single-Center-Studie analysierte [¹⁸F]FDG-PET/CT-Scans von 306 unbehandelten NSCLC-Patient:innen bei Erstdiagnose.
Referenzstandard: Manuelle Läsionssegmentierungen im Konsens zweier Hybrid-Imaging-Expert:innen.
- Befundung & Staging:
Durchführung mit der CE-zertifizierten, strukturierten Reporting-Plattform mint Lesion. - TNM-Klassifikation:
Nach der 9. Edition des TNM-Systems, unter Einbeziehung von Tumorboard-Entscheidungen. Die Klassifikation wurde durch mint Lesion semi-automatisiert durchgeführt, überprüft und als akkurat beurteilt.
- Befundung & Staging:
KI-Vergleich: Segmentierungen des leistungsstärksten Algorithmus aus dem autoPET III Challenge
- Klassifikation der Segmentierungsergebnise nach der 9. Edition des TNM-Systems
Die strukturierte, regelbasierte Segmentierung in mint Lesion ermöglicht eine zuverlässige semi-automatisierte TNM und UICC Klassifikation. Darüber hinaus stellt mint Lesion die technische Grundlage für die Studie dar, indem es die manuelle Segmentierung von Läsionen sowie den strukturierten Export der Daten für die anschließende Analyse ermöglicht.
Zentrale Ergebnisse der Studie
Technische Segmentierungsleistung
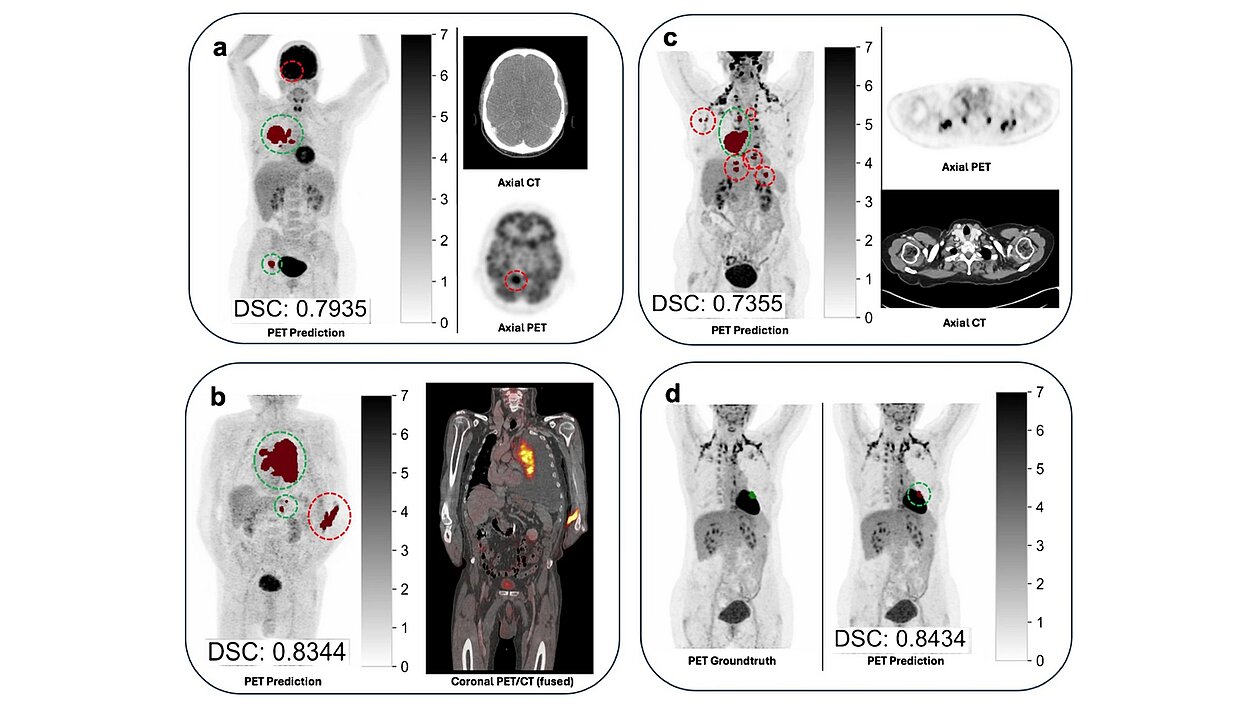
- Mittlerer Dice Similarity Coefficient (DSC): 0,64
- Systematische Volumenüberschätzung durch die KI (mittlere Differenz: +56,1 ml gegenüber manueller Segmentierung)
Läsionserkennung
- Sehr hohe Sensitivität auf Läsionsebene: 95,8%
- T-Kategorie: 96,7%
- N-Kategorie: 95,9%
- M- Kategorie 94,8%
Präzision und Fehlerursachen
- Moderate Präzision in der M-Kategorie (PPV: 73,7%)
- Häufigste Fehlerquelle: falsch positive Fernmetastasen
- 70,4% dieser falsch positiven M-Läsionen waren klinisch relevante, aber benigne oder nicht-onkologische Befunde, z. B.:
- degenerative muskuloskelettale Veränderungen
- entzündliche Prozesse wie Pneumonien
Auswirkungen auf das klinische Staging
- Übereinstimmung des UICC-Stadiums mit dem Goldstandard nur bei 67,4% der Patient:innen
- Upstaging bei 88 von 306 Fällen
- Hauptursachen:
- falsch positive M-Läsionen
- Untersegmentierung in der hilären Region
Klinische Einordnung und Schlussfolgerung
Die Studie kommt zu dem Schluss, dass der leistungsstärkste autoPET III-Algorithmus trotz der hervorragenden Sensitivität bei der Läsionserkennung (95,8%) nur eine Konkordanz von 67,6% für das UICC-Staging in NSCLC-Patienten aufwies, was auf erhebliche Einschränkungen für einen autonomen Einsatz hindeutet. Die klinische Relevanz der Segmentierungsfehler variiert stark, und das Upstaging durch falsch positive Läsionen war die primäre Ursache für die Staging-Diskrepanz.
Die Studie zeigt: Hohe technische Genauigkeit bedeutet nicht automatisch klinische Zuverlässigkeit.
Die Autor:innen empfehlen daher eindeutig:
- KI als Workflowoptimierung und -unterstützung, nicht als Ersatz
- Obligatorische ärztliche Kontrolle, insbesondere bei:
- M-Stadium-Vorhersagen
- komplexen Fällen mit multiplen Läsionen
Fazit
Die Studie unterstreicht die Bedeutung von aufgabenorientierter KI-Evaluation, die über reine Segmentierungsmetriken hinausgeht. Für die sichere klinische Integration von KI im onkologischen Hybrid-Imaging sind strukturierte Befundung, transparente Workflows und ärztliche Expertise unverzichtbar.
Für ein vollständiges Verständnis der Methodik, der detaillierten Fehleranalyse und der klinischen Implikationen wird die Lektüre der Originalpublikation empfohlen.
Diese Arbeit wurde vom Bundesministerium für Forschung, Technologie und Raumfahrt (BMFTR) im Rahmen der Fördermaßnahme „DataXperiment“ unterstützt (Projekt ID FKZ 01KD2431).
Heimer, Maurice M. et al. 2025. „Artificial intelligence for TNM staging in NSCLC: a critical appraisal of segmentation utility in [18F]FDG PET/CT”, European Journal of Nuclear Medicine and Molecular Imaging. https://doi.org/10.1007/s00259-025-07677-2.